
Ang mga simpleng eksperimentong teknikal ay kapaki-pakinabang na gawin sa mga bata, ito ay gumugugol ng oras nang magkasama, at pag-instill ng mga kasanayan, at pag-unawa sa pamamagitan ng maliliit na taga-disenyo, ang mga pangunahing kaalaman, na ang mga tinapay, tulad ng sa sikat na cartoon, ay hindi lumalaki sa mga puno.
Sa oras na ito, nagpasya kaming gawin ang pinakasimpleng kasalukuyang mapagkukunan ng kemikal, at subukang ilapat ito para sa anumang praktikal. Pinag-uusapan ang tungkol sa praktikal na aplikasyon, sulit na alalahanin na lamang ang ilang mga henerasyon na nakalipas, ang mga radio amateurs, upang matustusan ang kanilang mga tatanggap ng radio ng baterya at mga amplifier, ay inaalok upang gumawa ng ilang mga uri ng mga galvanic cell o baterya para sa independyenteng paggawa. Ito ang mga elemento ng Leklanshe at Popov [1] p. 9 ... 18, o isang lead-potash o gas baterya [1], p. 22 ... 28. Marami, ang medyo mataas na kasalukuyang elemento ay konektado sa isang maliwanag na baterya (maliwanag na maliwanag na filament ng mga tubo ng radyo), dose-dosenang mga mas maliit na elemento, sa isang baterya ng anode, ang boltahe kung saan maaaring umabot sa 60-80 volts. Ang mga baterya ay "basa" - na may likidong electrolyte at kinakailangang pangangalaga at pagpapanatili.
Kaya galvanic cell, ilang mga salitang "paano?" at "bakit?" Ang kasalukuyang electric ay nangyayari kapag nakikipag-ugnay ang mga metal. Sa kasong ito, ang isang iba't ibang mga potensyal na pagkakaiba-iba (boltahe) ay nangyayari. Bumalik noong 1793, si Alessandro Volta, na nagtatayo ng isang galvanic cell (Volta poste), itinatag ang kamag-anak na aktibidad ng mga kilalang metal na metal: Zn, Pb, Sn, Fe, Cu, Ag, Au. Ang "lakas" ng galvanic cell ay naging mas malaki, ang mas malayo na hiwalay ang mga metal sa hilera na ito ay tumayo (ang serye ng mga boltahe).

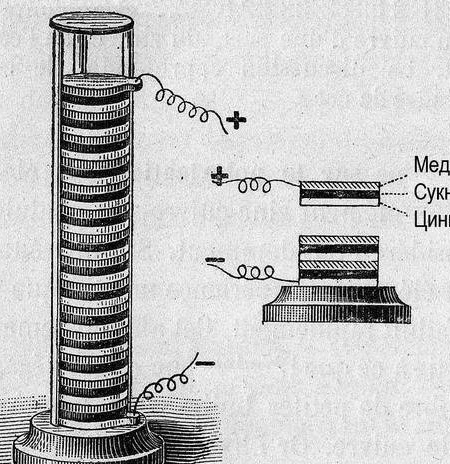
Nang maglaon, upang ayusin ang data, ang potensyal ng "hydrogen electrode" ay kinuha bilang isang sanggunian na zero. Matapos sukatin ang potensyal ng mga metal na ipinares sa kanya, ang mga eksperimentong metal ay inayos nang sunud-sunod. Ang nagresultang talahanayan ay tinawag na "Electrochemical series of metal stresses" at sa chemistry room, dapat mag-hang sa tabi ng pana-panahong system at ang larawan ni Dmitry Ivanovich.

Ang isang bilang ng mga metal na stress ay isang kapaki-pakinabang na pagbagsak, sa aming kaso, tulad namin, tulad ni Alessandro Volta, malalaman - ang karagdagang mga metal ay nahihiwalay sa bawat isa, mas malaki ang pag-igting na makuha.
Sa aming mga eksperimento, tulad ng mga klasiko, ginamit namin ang tanso at sink.Kapag ang mga plato ay nalubog sa isang electrolyte, sa pagitan nito at ng zinc plate, isang kemikal na reaksyon ang nangyayari, bilang isang resulta kung saan ang mga negatibong singil ay natipon sa plato at negatibong sisingilin. Bilang isang resulta ng reaksyon na nagaganap sa galvanic cell, ang zinc electrode ay unti-unting natutunaw.
Sa isang tanso na elektrod, sa panahon ng pagpapatakbo ng isang galvanic cell, ang maliliit na bula ng hydrogen ay nabuo na ibukod ang ibabaw ng tanso mula sa electrolyte. Ang kababalaghan ay tinatawag na, sa isang galvanic cell na ito ay nakakapinsala, nahihirapan sila dito. Upang alisin ang pinalabas na hydrogen, ang mga sangkap na tinatawag na hydrogen ay ipinakilala sa electrolyte. Sa kanilang papel ay madalas na mga compound ng mangganeso, tanso sulpate. Sa mga simpleng eksperimento, maaaring gamitin ang potassium permanganate ng parmasya.
Ang ginamit namin para sa eksperimento.
Mga aparato at materyales.
Para sa pagpupulong ng mga galvanic cells, bilang mga electrodes ng tanso, maaari mong gamitin ang wire, wire, foil. Ang zinc ay maaaring makuha mula sa mga tuyong elemento, maaaring magamit ang mga galvanized na produkto. Sa halip na sink, maaari mong subukang gumamit ng isang elektrod ng aluminyo o bakal. Ang sodium chloride para sa electrolyte, isang maliit na malambot na mounting wire. Tiyak na kailangan mo ng isang voltmeter o multimeter, wire cutter, gunting. Bilang mga vessel, maaaring magamit ang mga hindi lalagyan ng metal na angkop na sukat. Ang salamin, mas maginhawa kaysa sa mga light plastic na tasa - mas mabigat sila, mas matatag, mas mahirap kumatok. Napakabuti kung mayroong isang low-kasalukuyang low-boltahe na pag-load - isang simpleng radyo, isang relo ng kuwarts, atbp.
"Mataas na boltahe" na baterya ng kawad at mga turnilyo.
Nabighani sa pagiging simple ng mga detalye, at ang medyo mataas na boltahe na natanggap, sinubukan naming mag-ipon ng tulad ng isang baterya. Ang isang "klasikong" pares ng mga metal - tanso-zinc - ay ginagamit dito. Ang ideya ay ang paggamit ng mga galvanized fastener bilang isang zink elektrod. Mabuti na lamang. Malinaw na ang tulad ng isang elemento ay hindi idinisenyo para sa pangmatagalang operasyon - isang manipis na layer ng sink ay mabilis na matunaw, gayunpaman, hindi ito mahalaga para sa isang panandaliang eksperimento. Ngunit ang galvanized screws o cogs ay nasa lahat ng dako.
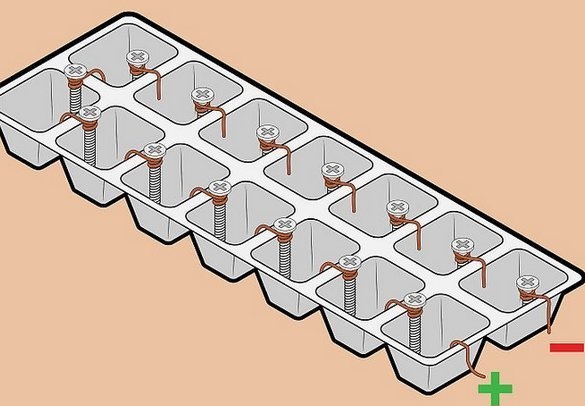
Ang isang wire ay ginagamit din bilang isang tanso elektrod - din ng isang malawak na magagamit na materyal, bilang karagdagan - ang pinaka-maginhawang pag-install ng mga elemento sa isang baterya - lahat ng mga elemento ay konektado sa serye - kasama ang isa sa minus ng susunod. Sa kasong ito, ang boltahe ay nakumpleto, ang kasalukuyang nananatiling pareho.
Magsimula tayo.
Matapos piliin ang kinakailangang bilang ng mga galvanized fastener ng nais na haba, nakita namin ang isang angkop na wire na tanso. Ito ay isang paikot-ikot na wire sa barnis pagkakabukod. Ang diameter ng kawad ay mga 0.5 mm.

Nililinis ng tuldok ang pagkakabukod ng barnisan, nang maraming beses, na may pagsusumikap sa paghila ng wire sa pamamagitan ng isang dobleng nakatiklop na paggiling balat ng daluyan na sukat.


Pagkatapos, naghahanda siya ng isang pares ng mga electrodes - sa ilalim ng ulo ng isang self-tapping screw, mahigpit na binabalot ang dalawa o tatlong mga liko ng wire at pinutol ang labis.

Ang pagpupulong ng baterya - isang trough ay ginamit bilang isang lalagyan para sa nagyeyelo na yelo. Maaari kang gumamit ng mga cell mula sa boxed sweets, gayunpaman, mas banayad ang mga ito. Matapos i-install ang mga electrodes sa mga pader sa pagitan ng mga cell, pinupuno namin ang mga lalagyan ng electrolyte. Gumamit kami ng isang solusyon ng salt salt - isang kutsara na may slide ng 0.5 litro ng maligamgam na tubig. Para sa pagpuno nito ay napaka-maginhawa upang gumamit ng isang medikal na hiringgilya.


Natagpuan namin ang ilang higit pang mga tornilyo para sa mga electrodes at idinagdag na mga elemento sa baterya, iyon ang nakuha namin. Ang boltahe sa isang mataas na impedance load (paglaban sa input ng isang digital voltmeter) ay malaki, ngunit sa anumang pagkarga, gayunpaman kapansin-pansin, bumaba ito nang malaki.
Subukang gawin magkakatulad na galvanic cell (baterya) na may mas malaking electrodes.
Bilang isang lalagyan, ginamit namin ang isang kalahating litro garapon (dalawa), ang mga plato ng isang malaking lugar ay magkasya sa loob nito. Bilang mga electrodes, kinuha namin ang manipis na tanso na foil at zinc - ang mga labi ng isang baso mula sa isang elemento na "tuyo" ng pabrika, na-disassembled sa panahon ng paggawa ng grapayt para sa pantunaw na patong.

Nilinis namin ang mga labi ng pinatuyong mga asing-gamot na mala-kristal na may brush ng wire at pinutol ang dalawang plato na may tinatayang gunting na may humigit-kumulang na parehong lugar. Mula sa foil ng tanso, gupitin ang dalawang magkatugma na guhitan. Gayundin sa gunting. Nakakuha kami ng dalawang pares ng mga electrodes, na nilagyan ang aming mga elemento, nang walang karagdagang ado, baluktot ang kanilang mga gilid sa leeg ng lata.


Sa isang mas malaking lalagyan, naghanda kami ng isang electrolyte - sodium klorido, natunaw sa maligamgam na tubig, pareho ang konsentrasyon, at inihanda ang mga elemento.


Ikinonekta namin ang dalawang elemento sa serye, gamit ang isang piraso ng mounting wire at dalawang clip ng buaya. Kaya, masarap, ang boltahe ng baterya ay malapit sa karaniwang "daliri", subukang gamitin. Ang isang elemento na may boltahe na 1.5 V ay ginagamit sa isang relo ng electromekanikal, bilang karagdagan, ang kasalukuyang pagkonsumo ng relo ay napakaliit at ang aming baterya ay magagawang madaig ito.

Inalis namin ang karaniwang baterya mula sa relo at nakakonekta sa mga terminal ng isang piraso ng mounting wire. Ang pag-obserba ng polarion (tanso na plato - "+", sink - "-"), na nakakonekta ang aming relo sa isang baterya ng makeshift, voila! Ang orasan ay gumagana, ang boltahe ay "lumubog" hanggang sa 1.3 V. Ang orasan ay gumana nang perpekto sa loob ng maraming oras, hanggang sa lahat tayo ay ipinagmamalaki (gayunpaman isang mangkukulam!) Pagkatapos ay napapagod kami.

Sa track.
Ang panloob na konstitusyon ng sinumang bata ay tulad ng pansin sa isang paksa, nagagawa niyang tumuon nang hindi hihigit sa 15 ... 20 minuto, at ang lahat ng mga klase na may mga bata ay dapat na binalak upang magkasya sila sa oras na iyon, o lumipat sa pagitan ng iba't ibang klase, kung hindi, pareho kayong mahihirapan.
Bilang isang pag-load, mas mahusay na mag-aplay na kung gumagalaw o maliwanag - ang mga numero sa voltmeter ay nagpapabilib sa isip, ngunit hindi ang puso. Bilang karagdagan sa mga relo at calculator, tiyak na magiging sanhi ito ng paghanga, ang gawain mula sa isang baterya na gawa sa bahay ng isang maliit na tatanggap ng radyo (bilang isang pagpipilian - isang yari sa bahay!).
Para sa pangmatagalang paggamit, ang electrolyte ng mga cell ay dapat maprotektahan mula sa alikabok at pagsingaw, at alagaan ang depolarizer - mabuti, hindi bababa sa pag-clog ng garapon na may isang piraso ng plastik na pelikula na may isang nababanat na banda at pagdaragdag ng potasa ng permanganeyt sa electrolyte. Bukod dito, mas mahusay na agad na kolektahin ang nabanggit na elemento ng Popov.
Bilang karagdagan sa galvanized self-tapping screws, posible na gumamit ng galvanized sheet steel, para sa mga malalaking elemento ito ay mas maginhawa - sa panahon ng eksperimento, makakakuha ka ng isang makabuluhang kasalukuyang at kapangyarihan anuman (paglipat ng iyong mga daliri sa hangin).
Listahan ng mga ginamit na panitikan.
1. P. Strelkov. Malaman at magagawang. Pinyerong de-koryenteng inhinyero. Detgiz. 1960 taon
2. V.S. Polosin, V.G. Prokopenko. Workshop sa pamamaraan ng pagtuturo ng kimika. Moscow, "Enlightenment", 1989, pp 202,203.

